|
М.И. Давыдов, М.Д. Тер-Ованесов Российский онкологический научный центр им. Н.Н. Блохина РАМН, Москва
В начало
Несмотря на стабильное снижение заболеваемости и летальности, рак желудка (РЖ) по-прежнему остается крайне актуальной проблемой человечества. Длительное время это грозное заболевание оставалось ведущей причиной смертности от онкологической патологии во всем мире. В последнее время благодаря изменениям пищевого рациона, методик приготовления и хранения пищи частота этого заболевания в экономически развитых странах постепенно снижается. Однако проблема раннего выявления и лечения РЖ на сегодняшний день остается высокоактуальной.
В настоящее время РЖ занимает второе место в структуре заболеваемости мужчин (14,7%) и третье в структуре заболеваемости женщин (10,8%) в России (В.И. Чиссов, 1998).
Уровень летальности от РЖ колеблется в различных регионах. Сравнительный анализ регионов с высоким и низким уровнем заболеваемости позволяет с некоторым приближением выделить ряд возможных этиологических факторов этого заболевания.
В настоящее время показано отсутствие достоверной связи заболевания с генетическими факторами (A. Neugut и соавт., 1995). Более сильным фактором, влияющим на частоту заболеваемости, является воздействие окружающей среды. Так, анализ показал, что при миграции из зоны с высоким уровнем заболеваемости в зону с низким уровнем частота развития РЖ снижается. Причем во втором поколении снижение более выражено, чем в первом (A. Nomura и соавт., 1990; K. Aoki, 1993).
Наиболее сильным экзогенным фактором риска является диета. Высококалорийная пища с включением животного мяса, копченостей, большим содержанием соли ассоциирована с высоким риском развития РЖ. В противоположность этому употребление свежих фруктов, клетчатки и витаминов (особенно бета-каротинов, витамина С) является защитным фактором (особенно для развития рака желудка интестинального типа) (S. Munoz и соавт., 1997; L. Harrison и соавт., 1997).
Одной из достоверных причин развития РЖ являются N-нитрозоамины, часто эндогенные. Пусковым моментом является снижение кислотности желудочного сока, встречающееся при хроническом гастрите и способствующее развитию патогенной флоры и увеличению синтеза нитросоединений в просвете органа (S. Leach и соавт., 1987).
В последние годы как достоверная рассматривается связь Helicobacter Pylori (H. Pylori) с развитием рака желудка. Сильнее эта корреляция проявляется при длительном периоде инфицирования в зонах повышенного риска (P. Sipponen, 1995), в старшей возрастной группе (M. Crespi, 1996; D. Graham, 1993).
Механизм H.Pylori-ассоциированного канцерогенеза связан со способностью микроорганизма вызывать выраженный инфильтративный гастрит с пролиферацией интерстициальных клеток. Длительный период воспаления вызывает процессы атрофии и кишечной метаплазии, которую следует рассматривать как предраковые изменения для развития РЖ кишечного типа. Несмотря на то, что диффузный тип РЖ не сочетается с кишечной метаплазией, H.Pylori-инфекция обнаруживается при диффузных карциномах в 100% наблюдений (D. Graham, 1993).
Другим инфекционным агентом, возможно связанным с развитием РЖ, является вирус Эпштейна-Барр (EBV): опухоли низкодифференцированные, с выраженной лимфоидной инфильтрацией. Такие опухоли описываются, как лимфоэпителиомоподобные раки. Технологии генной инженерии (методики гибридизации или полимеразной цепной реакции) EBV выявляют в 80% опухолей с лимфоидной стромой и в 6-9% низкодифференцированных аденокарцином без лимфоидной инфильтрации (S. Nakamura и соавт., 1994).
С развитием урбанизации на первое место среди факторов риска также вышли курение и употребление алкоголя (A. Nomura и соавт., 1990).
РЖ с повышенной частотой встречается при некоторых заболеваниях желудка, которые следует рассматривать как фоновые: хронический атрофический гастрит, хроническая язва желудка и культи желудка после дистальной резекции, аденоматозные полипы желудка, кишечная метаплазия и гиперпластическая гастропатия (S. Ming, 1998; F. Borchard, 1986; A. Gad, 1984). Обратная зависимость частоты ассоциации фоновых заболеваний и раннего РЖ была выявлена в Национальном Раковом Центре (Токио, Япония. S Ming и соавт. 1998). Эти данные представлены в табл. 1.
| Таблица 1. Фоновые заболевания РЖ |
| Фоновое заболевание |
Частота развития РЖ у пациентов с фоновыми заболеваниями (%) |
Частота выявления фоновых заболеваний у пациентов РЖ (%) |
| Хронический атрофический гастрит |
0-13 |
94,8 |
| Пернициозная анемия |
0,5-12,3 |
- |
| Хроническая язва желудка |
1-2 |
0,7 |
| Гиперпластический полип |
1-2 |
0,5 |
| Плоская аденома |
6-21 |
2,5 |
| Папилловирусная аденома |
20-75 |
- |
| Болезнь Менетрие |
5-10 |
- |
| Резекция желудка в анамнезе |
0,4-7,8 |
0,7 |
Некоторые успехи комбинированных методов лечения, именно хирургическое лечение остается "золотым" стандартом при радикальном лечении злокачественных опухолей желудочно-кишечного тракта (ЖКТ), позволяющем надеяться на полное выздоровление.
Традиционно радикальные операции по поводу рака различной локализации включали обязательное моноблочное удаление регионарных лимфатических узлов. Впервые такой подход был предложен более 100 лет назад Holsted при хирургическом лечении рака молочной железы. С тех пор этот стандарт применялся и при хирургическом лечении рака ЖКТ различных локализаций.
Понятие превентивной расширенной лимфодиссекции было впервые введено при хирургическом лечении РЖ для обозначения операций, сопровождавшихся плановым удалением пораженного органа и зон регионарного метастазирования. Следует акцентировать внимание, что термин "лимфодиссекция", являясь более емким, чем термин "лимфаденэктомия", включает моноблочное удаление не только лимфатических узлов, но и всего лимфатического аппарата (лимфатических сосудов с окружающей жировой клетчаткой) в пределах фасциальных футляров.
Именно это положение, обоснованное временем и опытом, является теоретической предпосылкой возможности выполнения радикальной операции при РЖ путем удаления первичного очага с зонами возможного (с высокой степенью вероятности) регионарного лимфогенного метастазирования. Причем первое положение - улучшение локального контроля со снижением возможности местного рецидива - также заключает в себе и другую предпосылку - возможность определения истинной распространенности процесса. Действительно, в случае широкого лимфогенного метастазирования, а также при других стигмах распространенности можно с высокой степенью вероятности говорить о наличии субклинической диссеминации процесса. Это, с одной стороны, обусловлено возможностью нарушения фильтрации опухолевых клеток лимфатическими узлами с распространением в системный кровоток, а с другой стороны - наличием экстраорганных лимфатических и прямых лимфатико-гематогенных шунтов, обусловливающих возможность ранней лимфогематогенной диссеминации. Однако при отсутствии данных, свидетельствующих о распространенности процесса, достоверно оценить стадию заболевания, а также выполнить радикальное вмешательство возможно лишь при удалении зон регионарного лимфогенного метастазирования.
В литературе описаны лишь несколько проспективных рандомизированных исследований, позволяющих полноценно оценить истинную значимость расширенного объема лимфодиссекции в хирургическом лечении РЖ. Поэтому большинство хирургических клиник ориентируется лишь на теоретическую эффективность моноблочного удаления первичного очага и зон лимфогенного метастазирования, свои ощущения и многолетний опыт, а также на данные об улучшении отдаленных результатов, публикуемых ведущими клиниками мира, в первую очередь японскими.
Впервые моноблочное удаление зон регионарного метастазирования с первичным очагом при РЖ с целью улучшения отдаленных результатов было рекомендовано в начале 60-х годов Jinnai и соавт. С этого момента концепция радикальной расширенной лимфодиссекции при РЖ как обязательном интегрированном этапе операции стала применяться в Японии. Исследования по топографии, методологии и практической значимости расширенной лимфодиссекции легли в основу первого издания Основных правил по изучению рака желудка (General Rules for Gastric Cancer Study), вышедшего в свет в 1963 г. под редакцией Японского исследовательского общества по изучению рака желудка (Japanese Research Society for Gastric Cancer - JRSGC). Первое европейское издание на английском языке, доступное гастроэнтерологам мира в их работе, вышло лишь в 1995 г. и было основано на 12-й переработанной редакции Правил.
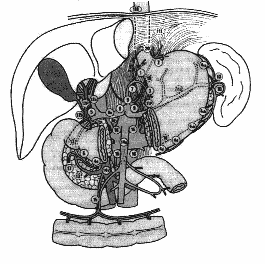
В настоящее время на основании работ JRSGC (1998) детально описаны 16 групп регионарных лимфатических узлов, формирующих четыре последовательные (не в истинном понимании последовательности) этапа метастазирования от различных отделов желудка - N1 до N4 (рис. 1):
 |
|
| Рис.1. Схема регионарных лимфатических узлов желудка (Japanese Research Society for Gastric Cancer 1998). |
- Первый этап: перигастральные лимфоколлекторы, расположенные в связочном аппарате желудка (1-6);
- Второй этап: лимфатические узлы по ходу артериальных стволов: левой желудочной артерии (7), общей печеночной артерии (8a+р), чревного ствола (9), в воротах селезенки (10), по ходу селезеночной артерии (11);
- Третий этап: лимфатические узлы гепатодуоденальной связки (12a+p+b), ретропанкреатодуоденальные (13), корня брыжейки поперечноободочной кишки (14);
- Четвертый этап: лимфатические узлы по ходу верхней брыжеечной артерии (15), парааортальные (16).
Далее...
Написать комментарий
|

