|
Катруха Г.С., Федорова Г.Б., Архангельская Н.М., Яссеин М., Лайко А.В., Трифонова Ж.П. Научно-исследовательский институт по изысканию новых антибиотиков Российской АМН, Москва
АНТИБИОТИКИ И ХИМИОТЕРАПИЯ, 1999-N5, стр. 6-11.
В начало...
(Окончание)
Отнесение выделенных антибиотиков к группе полипептидов сделано после анализа кислотных и щелочных гидролизатов компонентов. Поскольку УФ-спектры компонентов указывали на присутствие в молекуле индольных радикалов, был проведен также восстановительный кислотный гидролиз в 6 н. НСl в присутствии 4% тиогликолевой кислоты.
В результате анализа кислотных и щелочных гидролизатов методами ТСХ на силикагеле (система Т-1), электрофореза на бумаге при рН 2,4 (Е-2) и 4,3 (Е-4) и на автоматическом аминокислотном анализаторе было установлено, что в состав каждого из анализируемых антибиотиков входят белковые аминокислоты (число остатков): Ser (1), Glu (1), Gly (2), Ala (1), Val (2), lle (2), Leu (1), Trp (1) и две небелковых аминокислоты (Х1 и Х2), содержащих серу. Присутствие одного остатка Trp подтверждено методом спектрофотометрического титрования с NBS. Аминокислоты Х1 и Х2 были идентифицированы как лантионин (Lan) и 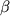 -метиллантионин ( -метиллантионин (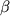 -MeLan)соответственно после их препаративного выделения из гидролизата антибиотика методом хроматографии на бумаге и последующего масс-спектрометрического анализа (FAB-MS) и ТСХ анализа в системах Т-1 и Т-2 со свидетелями Lan и -MeLan)соответственно после их препаративного выделения из гидролизата антибиотика методом хроматографии на бумаге и последующего масс-спектрометрического анализа (FAB-MS) и ТСХ анализа в системах Т-1 и Т-2 со свидетелями Lan и 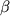 -MeLan. Аминокислотный состав изучаемых компонентов антибиотика 3802 представлен в табл. 2. Из данных таблицы следует, что по аминокислотному составу компоненты антибиотика А-3802 практически не различаются между собой. Лишь в компоненте А-3802-IV-4 обнаруживается цистеиновая кислота (CySO3H), образовавшаяся, очевидно, из сульфона (сульфоксида) лантионина при кислотном гидролизе. -MeLan. Аминокислотный состав изучаемых компонентов антибиотика 3802 представлен в табл. 2. Из данных таблицы следует, что по аминокислотному составу компоненты антибиотика А-3802 практически не различаются между собой. Лишь в компоненте А-3802-IV-4 обнаруживается цистеиновая кислота (CySO3H), образовавшаяся, очевидно, из сульфона (сульфоксида) лантионина при кислотном гидролизе.
| Таблица 2. Аминокислотный состав некоторых компонентов антибиотика А-3802 и актагардина (число остатков/моль) |
| Аминокислота |
А-3802-IV-3 |
A-3802-IV-4 |
A-3802-V-4 |
A-3802-VI-7 |
Актагардин |
| Ser |
1 |
1 |
1 |
1 |
1 |
| Glu |
1 |
1 |
1 |
1 |
1 |
| Gly |
2 |
2 |
2 |
2 |
2 |
| Ala |
1 |
1 |
1 |
1 |
1 |
| Val |
2 |
2 |
2 |
2 |
2 |
| lle |
2 |
2 |
2 |
2 |
2 |
| Leu |
1 |
1 |
1 |
1 |
1 |
| Trp |
1 |
1 |
1 |
1 |
1 |
| Lan |
1 |
1 |
1 |
1 |
1 |
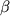 -MeLan -MeLan |
2 |
- |
2 |
2 |
2 |
Ala-SO-Abu (сульфоксид 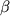 -MeLan) -MeLan) |
1 |
3 |
1 |
1 |
1 |
| Мол. масса |
1889 |
1919 |
1931 |
1945 |
1889 |
Таким образом, результаты ВЭЖХ смеси компонентов, их аминокислотного и масс-спектрометрического анализа и хроматографического и электрофоретического анализа в различных электролитах свидетельствуют, что основным компонентом антибиотического комплекса А-3802 является компонент А-3802-IV-3 с молекулярной массой 1889 Да. Компонент А-3802-IV-4 с мол. массой 1919 Да представляет собой диамид-дисульфоксид основного компонента А-3802-IV-3, компонент А-3802-V-4 - N-ацетильное производное основного компонента, а компонент А-3802-VI-7 - метиловый эфир компонента А-3802-V-4.
Для подтверждения строения последних двух компонентов мы провели обработку антибиотика А-3802-IV-3 уксусным ангидридом в метаноле, а часть полученного N-ацетильного производного - смесью МеОН/НСl для его этерификации. Продукты модификации исследовали методами ТСХ и FAB-MS. Результаты анализа представлены в табл. 3. Данные табл. 3 подтверждают выводы о строении компонентов А-3802-V-4 и VI-7.
| Таблица 3. Сравнение некоторых свойств двух новых компонентов антибиотика А-3802 и продуктов направленной модификации основного компонента А-3802-IV-3 |
| Соединение |
ТСХ в системе Т-3 (Rf) |
FAB-MS (M+H)+ |
| A-3802-V-4 |
0,45 |
1932 |
| A-3802-IV-3 + (CH3CO)2O |
0,47 |
1932 |
| A-3802-VI-7 |
0,63 |
1946 |
| A-3802-IV-3 + (CH3CO)2O + CH3OH/HCl |
0,63 |
1946 |
Важным этапом в исследовании антибиотиков-полипептидов является определение их N-концевых аминокислот. Однако применение распространенных в пептидной химии ДНФ- и ДНС-методов не дало положительных результатов: полного модифицирования свободной аминогруппы компонента А-3802-IV-3 достичь не удалось. Очевидно, аминогруппа стерически недоступна для таких объемных реагентов, как 2,4-динитро-1-фторбензол и 1-диметиламинонафталин-5-сульфохлорид. В дальнейшем мы использовали низкомолекулярный и высокоактивный реагент - метилизотиоцианат (МИТЦ, СН3-N=C=S), который применяется для определения N-концевой последовательности пептидов и белков [16, 17]. Электрофоретический анализ в электролите Е-1 продуктов реакции метилтиокарбамилирования (1 стадия) и циклизации (2 стадия, расщепление пептидной связи) показал, что обе реакции проходят полностью. Однако методом ТСХ было установлено, что отщепления N-концевой аминокислоты не произошло, что указывает на N-концевое расположение лантионина или 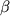 -метиллантионина. Действительно, в кислотном гидролизате МТГ-3802-IV-3 полностью отсутствовал лантионин, который, следовательно, занимает в молекуле антибиотика N-концевое положение. После второго цикла отщепления с использованием МИТЦ методом ТСХ со свидетелями был идентифицирован МТГ-серин. Следовательно, антибиотик А-3802-IV-3 имеет на N-конце последовательность -метиллантионина. Действительно, в кислотном гидролизате МТГ-3802-IV-3 полностью отсутствовал лантионин, который, следовательно, занимает в молекуле антибиотика N-концевое положение. После второго цикла отщепления с использованием МИТЦ методом ТСХ со свидетелями был идентифицирован МТГ-серин. Следовательно, антибиотик А-3802-IV-3 имеет на N-конце последовательность 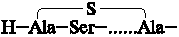 . .
Для идентификации полученных антибиотиков мы провели поиск аналогов по компьютерной базе данных природных биологически активных веществ (BNPD), разработанной Я. Берди (Венгрия) [18]. Поиск вели путем введения в компьютер полученных аналитических данных по мол. массе, УФ-спектру и элементарному составу компонентов антибиотика А-3802. Результаты анализа базы данных позволили установить, что антибиотик А-3802-IV-3 практически по всем дескрипторам идентичен актагардину (гардимицину) [19-21] - 19-членному лантибиотику с четырьмя пептидными циклами, образованными тиоэфирными связями лантионина и 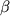 -метиллантионина (3 остатка), строение которого установлено в 1990-1995 гг. [22, 23] (рис. 2), а компонент А-3802-IV-4 - диамиду актагардина [22]. Сведения об антибиотиках-полипептидах с мол. массой 1932 и 1945 Да в базе данных BNPD и в доступной литературе отсутствуют и поэтому можно считать, что выделенные нами из антибиотического комплекса компоненты А-3802-V-4 и А-3802-VI-7 являются новыми антибиотиками. В табл. 4 приведены сравнительные данные по биологи-ческой активности полученных антибиотиков. -метиллантионина (3 остатка), строение которого установлено в 1990-1995 гг. [22, 23] (рис. 2), а компонент А-3802-IV-4 - диамиду актагардина [22]. Сведения об антибиотиках-полипептидах с мол. массой 1932 и 1945 Да в базе данных BNPD и в доступной литературе отсутствуют и поэтому можно считать, что выделенные нами из антибиотического комплекса компоненты А-3802-V-4 и А-3802-VI-7 являются новыми антибиотиками. В табл. 4 приведены сравнительные данные по биологи-ческой активности полученных антибиотиков.
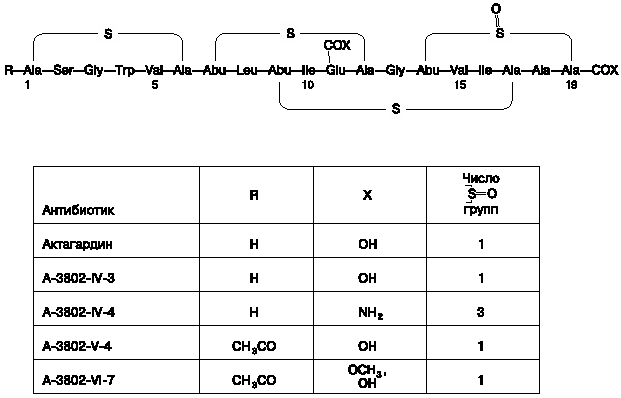 |
| Рис. 2. Строение актагардина и компонентов антибиотического комплекса А-3802. |
| Таблица 4. Антибиотическая активность компонентов антибиотика А-3802 и актагардина в отношении Bacillus mycoides |
| Антибиотик |
МПK, мкг/мл* |
| А-3802-IV-3 |
0,31 |
| A-3802-V-4 |
0,39 |
| A-3802-VI-7 |
0,17 |
| Актагардин |
0,25 |
Примечание. * Определение методом серийных разведений.
Из табл. 4 видно, что полученные нами антибиотики, несмотря на некоторые структурные различия, обладают близкой антибиотической активностью, сравнимой с активностью актагардина. Известно, что лантибиотики, к которым относятся такие антибиотики, как низин, субтилин, эпидермин, анковенин, дюрамицин, мерсацидин, актагардин и др., являются бактериоцинами, активными в отношении грамположительных бактерий [24]. Они образуются в результате посттрансляционной модификации рибосомально-синтезируемого предшественника лантибиотиков [25]. В последние годы наблюдается повышенный интерес к этим полипептидам из-за их потенциального применения в качестве консервантов продуктов питания и терапевтических агентов. Детально изучается механизм биосинтеза лантибиотиков и бактерицидного действия на клеточном уровне, а также их конформационные особенности. Известно также, что актагардин является ингибитором некоторых ферментов, обладает способностью подавлять биосинтез пептидогликана клеточной стенки бактерий и малотоксичен. Антибиотики с такими свойствами представляют интерес для биохимиков и практической медицины, и поэтому работы по изучению строения и взаимосвязи между строением и биологической активностью в ряду компонентов антибиотического комплекса А-3802 будут продолжены.
Авторы приносят большую благодарность д-ру Giancarlo Lancini (Gruppo Lepetit, Милан, Италия) за любезно предоставленный образец актагардина, Н.Л. Токаревой за ВЭЖХ анализ компонентов антибиотика А-3802, Н.М. Малютиной за снятие ИК-спектров антибиотика и РФФИ за частичную финансовую поддержку данного исследования (грант N 94-04-12589).
1.Из культуральной жидкости продуцента Actinoplanes brasiliensis ИНА 3802 выделен антибиотический комплекс А-3802, из которого методами экстракции органическими растворителями и хроматографии получены 4 антибиотика - А-3802-IV-3, А-3802-IV-4, А-3802-V-4 и А-3802-VI-7.
2.Показано, что антибиотики А-3802-IV-3 и А-3802-IV-4 идентичны с антибиотиками группы лантибиотиков актагардином и дисульфоксидом его диамида соответственно, а антибиотики А-3802-V-4 и А-3802-VI-7 являются новыми представителями этой же группы антибиотиков.
3.Выделенные антибиотики имеют близкую антибактериальную активность в отношении некоторых грамположительных бактерий.
АНТИБИОТИКИ И ХИМИОТЕРАПИЯ, 1999-N5, стр. 6-11.
1. Лайко А.В., Терехова Л.П., Сумарукова И.Г. и др. Актуальные направления поисков антибиотиков: Тез докл II-го Всесоюз сем. Алма-Ата 1989; 25.
2. Терехова Л.П., Галатенко О.А., Лайко А.В. и др. Антибиотики и химиотер 1999; 4: 5-8.
3. Katrukha G.S., Trifonova Zh.P., Yassein M.E. et al. International Organic Substances Solvent Extraction Conference Sept., 22-25, Voronezh, Russia, 1992; 11: 155-156.
4. Durrum E.L. J Amer Chem Soc 1950; 72: 2943-2944.
5. Степанов В.М., Силаев А.Б., Катруха Г.С. Биохимия 1960; 25: 749-756.
6. Хроматография на бумаге./Под ред И.М. Хайса и К. Мацека. М 1962.
7. Бэйли Д. Методы химии белков. М: Мир 1965; 284.
8. Практическая химия белка./Под ред А. Дарбре. М: Мир 1989; 621.
9. Matsubara H., Sasaki R.M. Biochem Biophys Res Commun 1969; 35: 175-181.
10. Блок Р. Аналитические методы белковой химии. М 1963; 470.
11. Gross E., Kiltz H.H., Craig L.C., Hoppe-Seyler's Z. Physiol Chem 1973; 354: 799-801.
12. Myhill D., Jackson D.S. Anal Biochem 1963; 6: 2.
13. Delaney R. Anal Biochem 1972; 46: 413-420.
14. Patchornik A., Lawson W., Witkop B. J Amer Chem Soc 1958; 80: 4747-4749.
15. Дэвени Е., Гергей Я. Аминокислоты, пептиды и белки. М: Мир 1976.
16. Степанов В.М., Кривцов В.Ф. Журн общей химии 1965; 35: 53-57.
17. Амирханян М.М., Степанов В.М. Биохимия 1970; 35: 825-830.
18. Berdy J. Abstr of Intern Conf on Microbial Secondary Metabolites. Okt 5-8. Interlaken Suisse 1994; 2.
19. Parenti F., Pagani H., Beretta G. J Antibiot 1976; 29: 501-506. 20. Coronelli L., Tamoni G. Ibid 507-510.
21. Malabarba A., Landi M., Pallanza R., Cavalleri B. Ibid 1985; 38: 1506-1511.
22. Kettenring J.K., Malabarba A., Vekey K., Cavalleri B. Ibid 1990; 43: 1082-1088.
23. Zimmermann N., Mitzger G.W., Jung G. Eur J Biochem 1995; 228: 786-797.
24. Van de Ven F.J.M., Jung G. Antonie van Leeuwenboek 1996; 69: 99- 107.
25. de Vos W.M., Kuipers O.P. Mol Microbiol 1995; 17: 427-437.
Написать комментарий
|

