|
Яковлев С.В. Московская медицинская академия им. И.М.Сеченова
В начало...
Связь терапевтического эффекта и концентрации лекарства в крови - важная проблема современной медицины для обоснования наиболее эффективного режима дозирования и применения лекарственного препарата. Успехи клинической фармакологии последних десятилетий позволили вплотную подойти к количественному анализу закономерностей, связывающих терапевтические или токсические эффекты с концентрацией препарата в крови и тканях [1, 2, 3, 4]. Для количественного описания связи "эффект - концентрация" используют различные функциональные зависимости (линейную, логарифмическую, гиперболическую и др.), при этом применяют данные о концентрации лекарственных средств в плазме (сыворотке) крови, различных тканях, камерах многочастевых моделей, в так называемой "эффекторной камере" и т.д. Чаще всего эмпирически подбирают ту функциональную зависимость и ту "биофазу", которые обеспечивают наилучшую корреляцию "эффект - концентрация" [1]. В частности, такая связь между концентрациями лекарств и выраженностью фармакодинамического эффекта довольно точно установлена для многих препаратов (антиаритмические средства, сердечные гликозиды, психотропные средства и др.), что лежит в основе фармакокинетического контроля при фармакотерапии различных заболеваний.
Труднее установить количественную зависимость между концентрациями лекарств в крови/тканях и выраженностью терапевтического эффекта в клинической антимикробной химиотерапии, так как последняя, в отличие от клинической фармакологии, рассматривает взаимодействие не двухкомпонентной (лекарство - организм человека), а трехкомпонентной системы: лекарство - микроорганизм - организм человека (макроорганизм). Степень воздействия антибактериального средства на микроорганизм количественно описывается величиной МПК (минимальная подавляющая концентрация) и МБК (минимальная бактерицидная концентрация), которые зависят от вида микроорганизма (т.е. природной резистентности) и его вторичной, индуцибельной резистентности. Кроме того, значения МПК и МБК определяются на основании данных, полученных in vitro, в то время как инфекционный процесс протекает в организме человека, и многие другие факторы (локализация инфекции, рН в месте инфекции, величина микробной нагрузки, состояние защитных сил макроорганизма, взаимодействие антибактериальных и других лекарственных средств) также могут оказывать влияние на величину фармакодинамического эффекта. Все перечисленное объясняет сложность установления прямой зависимости между концентрацией препарата в крови/тканях и клиническим эффектом в химиотерапии.
Ранние исследования в химиотерапии по связи фармакокинетики и фармакодинамики были связаны с установлением зависимости между концентрацией антибиотика в крови и выраженностью его токсических эффектов. В частности, такая зависимость была установлена для нефро- и ототоксических эффектов аминогликозидов [5] и нефротоксических эффектов ванкомицина [6]. В дальнейшем на основании экспериментальных исследований in vitro и in vivo была показана возможность установления количественной зависимости между концентрациями антибактериальных средств в крови/тканях и выраженностью их клинического эффекта [7 - 10]. Эта зависимость имеет различные характеристики для разных групп антимикробных средств.
Фторхинолоны характеризуются быстрым бактерицидным действием, прямо зависящим от их концентрации в крови. При этом клиническая эффективность фторхинолонов является функцией не только величины максимальной концентрации Cмакс, но и времени, в течение которого концентрации препарата в крови превышают МПК. В экспериментальных и клинических исследованиях установлено, что параметром, наиболее точно прогнозирующим эффективность фторхинолонов, является отношение величины площади под фармакокинетической кривой "концентрация - время" в интервале 0-24 часа, обычно обозначаемой в литературе как АUС0-24, и принятой нами как ППК к значению МПК [11]. Этот интегральный параметр можно обозначить как ППК/МПК.
В исследовании A. Forrest [12] было показано, что адекватный клинический эффект (80% и выше) при применении ципрофлоксацина у тяжелых больных в реанимации может быть достигнут при значениях ППК/МПК, превышающих 125 (рис. 1). В этом же исследовании были рассчитаны дозы ципрофлоксацина, при которых ожидается адекватный клинический и бактериологический эффекты при выделении различных микроорганизмов (табл. 1). В отношении высокочувствительных штаммов, для которых МПК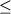 0,2 мкг/мл, достаточной является суточная доза ципрофлоксацина 600 (ППК/МПК>125). При выделении менее чувствительных штаммов (Staphylococcus aureus, Pseudomonas aeruginosa, при МПК 0,5 мкг/мл) для достижения адекватного эффекта (ППК/МПК 0,2 мкг/мл, достаточной является суточная доза ципрофлоксацина 600 (ППК/МПК>125). При выделении менее чувствительных штаммов (Staphylococcus aureus, Pseudomonas aeruginosa, при МПК 0,5 мкг/мл) для достижения адекватного эффекта (ППК/МПК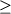 125) требуется увеличение суточной дозы ципрофлоксацина до 1200 мг. 125) требуется увеличение суточной дозы ципрофлоксацина до 1200 мг.
 |
Рис 1. Зависимость между эффективностью (клинической и бактериологической) и величиной ППК/МПК ципрофлоксацина [12].
Черный столбец - бактериологический эффект, серый столбец - клинический эффект. |
В другом исследовании [13] было показано, что предупредить развитие устойчивости у бактерий в процессе лечения можно, если значения ППК/МПК ципрофлоксацина будут превышать 100.
Таким образом, можно предположить, что при применении фторхинолонов гарантом адекватного клинического и бактериологического эффектов является достижение значения ППК/МПК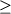 100. 100.
В опубликованных нами ранее исследованиях [14, 15] было показано значение фармакокинетических исследований в оптимизации режима дозирования ломефлоксацина у больных с терминальной почечной недостаточностью, получающих лечение гемодиализом. В настоящем исследовании мы поставили задачу определить оптимальный режим дозирования ломефлоксацина у больных с внебольничными инфекциями нижних дыхательных путей, используя фармакокинетические и фармакодинамические подходы.
Ломефлоксацин обладает высокой активностью в отношении грамотрицательных бактерий, являющихся возбудителями внебольничных инфекций нижних дыхательных путей (МПК90 для H.influenzae и M. catarrhalis составляют <0,25 мкг/мл, для большинства бактерий семейства Enterobacteriaceae - 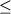 0,5 мкг/мл);в отношении P.aeruginosa диапазон значений МПК90 составляет 2-8 мкг/мл (в среднем 4 мкг/мл) [16-18]. Активность ломефлоксацина в отношении грамположительных микроорганизмов (стафилококков, стрептококков) менее выражена (МПК90>1 мкг/мл). Главным недостатком ломефлоксацина (как и других, "классических", фторхинолонов) является невысокая активность в отношении ведущего возбудителя внебольничных инфекций дыхательных путей - Streptococcus pneumoniae (МПК90 составляет от 2 до 8 мкг/мл), что лимитирует его применение при этой патологии. В большом многоцентровом исследовании 31% штаммов пневмококков были устойчивы к ломефлоксацину [19]. 0,5 мкг/мл);в отношении P.aeruginosa диапазон значений МПК90 составляет 2-8 мкг/мл (в среднем 4 мкг/мл) [16-18]. Активность ломефлоксацина в отношении грамположительных микроорганизмов (стафилококков, стрептококков) менее выражена (МПК90>1 мкг/мл). Главным недостатком ломефлоксацина (как и других, "классических", фторхинолонов) является невысокая активность в отношении ведущего возбудителя внебольничных инфекций дыхательных путей - Streptococcus pneumoniae (МПК90 составляет от 2 до 8 мкг/мл), что лимитирует его применение при этой патологии. В большом многоцентровом исследовании 31% штаммов пневмококков были устойчивы к ломефлоксацину [19].
Максимальные концентрации ломефлоксацина в крови составляют 3-5,2 мкг/мл после приема внутрь 400 мг. Препарат в незначительной степени связывается с белками плазмы и хорошо проникает в различные ткани, в том числе в слизистую бронхов, альвеолы и мокроту, концентрации в которых составляют 89-200% от сывороточных [18, 20]. Период полувыведения ломефлоксацина составляет в среднем 8 часов. В эксперименте показано и в клинических исследованиях подтверждено, что ломефлоксацин может применяться с интервалом 24 часа [18, 21].
Далее...
Написать комментарий
|

