|
Некоторые актуальные проблемы патогенеза
гнойной раны
Сергей Алексеевич Писаржевский
Клинико-биохимическая лаборатория,
Институт хирургии им. А.В.Вишневского РАМН.
Содержание
1.Введение.
Гнойная рана - чрезвычайно
сложное и многоплановое явление. В изучении
ее патогенеза основной вклад вносят
микробиология, биохимия, цитология и
иммунология. В настоящее время наибольшее
внимание исследователей вызывают
следующие проблемы, имеющие
фундаментальный характер :факторы
микроорганизмов, оказывающие влияние на
другие микроорганизмы и на макроорганизм,
системы антибактериальной защиты
организма, роль медиаторов и антимедиаторов
воспаления в раневом инфекционном процессе,
взаимодействие клеточных популяций в
гнойной ране, регуляция иммунного ответа
при гнойной инфекции. В практическом плане
важна разработка принципов
патогенетического лечения гнойных ран и их
осложнений, в том числе при заболеваниях,
отягчающих течение инфекционного процесса
в ранах. Для повышения надежности прогноза
нагноения ран и течения инфекции в них, а
также для оптимизации лечения гнойных ран
полезным явилось бы создание модели
гнойной раны (в идеале в виде компьютерной
программы). Указанным выше вопросам и
посвящен настоящий обзор.
2. Основные возбудители гнойных
хирургических инфекций.
В настоящее время основными
возбудителями гнойных хирургических
инфекций считаются стафилококки
и грамотрицательные бактерии,
принадлежащие к семейству Enterobacteriacea
и к обширной группе так называемых неферментирующих
бактерий. Существенную роль в
этиологии раневой инфекции отводится облигатным
неспорообразующим анаэробным
бактериям (подробнее, а также об особых
видах раневой инфекции см /22/).
3. Роль бактерий в раневом
инфекционном процессе.
Роль бактерий в раневом
инфекционном процессе неоднозначна. С
одной стороны, они вырабатывают факторы
патогенности. К ним прежде всего следует
отнести факторы инвазивности, т.
е. факторы, способствующие внедрению
микробов в живые ткани. Классическим
фактором инвазивности считается гиалуронидаза
(3. 2. 1. 35 и 4. 2. 2. 1)
стафилококков /11/. St.
aureus продуцирует белки, связываюшиеся с
белками матрикса, тканей и плазмы,
такими как фибронектин, фибриноген,
коллаген, эластин, плазминоген
и др. Эти белки способствуют колонизации
бактериями тканей раны /46/.
Ps. aeruginosa образует
специфические адгезины для ламинина-компонента
базальной мембраны, что способствует
обсеменению этой бактерией поврежденных
тканей /47/.
Бактерии вырабатывют токсины.
В качестве примеров можно привести
и 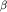 токсины
стафилококков, гемолизин стрептококков,
эндотоксин грамотрицательных бактерий /11/,
а также низкомолекулярные токсические
вещества (фенол, индол
и др.)/22/. токсины
стафилококков, гемолизин стрептококков,
эндотоксин грамотрицательных бактерий /11/,
а также низкомолекулярные токсические
вещества (фенол, индол
и др.)/22/.
Бактерии продуцируют факторы,
угнетающие иммунитет. Так,
например, некоторые бактерии секретируют
факторы, препятствующие слиянию фагосом
с лизосомами /17/, лейкоцидин
стафилококков вызывает гибель полинуклеарных
лейкоцитов /11/, Ps. aeruginosa продуцирует супероксид-дисмутазу,
что способствует устойчивости бактерии к
генерируемуму фагоцитами макроорганизма супероксиду
/48/,стрептококки группы А образуют гиалуронатную
капсулу, препятствующие опсонизации
и фагоцитозу /28/.
К факторам патогенности следует
также причислить суперантигены.
Суперантигеном называется
бифункциональная молекула, реагирующая со
сравнительно неизменными областями Т-клеточных
рецепторов и с молекулами главного
комплекса гистосовместимости класса II на
специализированных клетках, включая В-клетки
и моноциты. Суперантигены вызывют
усиленную пролиферацию Т-клеток. Как и
липополисахариды грам-отрицательных
бактерий, так и суперантигены грам-положительных
бактерий вызывают усиленную продукцию
цитокинов и являются одними из главных
факторов,вызывающих сепсис и септический
шок /40, 45, 50/.
Здесь же следует упомянуть о
явлении микробной мимикрии. В случаях
наличия общих антигенов у человека и
паразитирующих в его организме микробов
они могут быть следствием антигенной
мимикрии паразита, облегчающего его
инвазию и преодаление иммунитета. Эволюция
неизбежно должна вести селекцию таких форм
паразитов, которые все более и более
уподобляются антигенам хозяина и
становятся "невидимыми" для иммунитета.
Антигенная мимикрия не только блокирует
образование антител к чужеродным антигенам,
но и нарушает толерантность к собственным
антигенам человека, провоцируя тяжелые
аутоиммунные заболевания. Например, один из
белков St. aureus сходен с изоантигенами
эритроцитов группы А. Из-за этого
предрасположенность к септицимии
и хронизации стафилококковой инфекции у
больных с группой крови А значительно
больше по сравнению с больными, имеющими
группу крови В. Болезнетворные бактерии
преодалевают тканевые барьеры хозяина,
контактируя с поверхностными структурами
клеток, и одним из механизмов этого
процесса является антигенная мимикрия:
лиганды бактерий имеют фрагменты молекул,
аналогичные связывающим сайтам некоторых
естественных физиологически активных
веществ человека. Например, адгезины
E.coli содержат домены,специфически
реагирующие с ганглиозидами, которые
исходно предназначены для восприятия
сигналов от пептидных гормонов. У E.coli, St. aureus
oбнаружены белки, имитирующие инсулин,
гонадотропин, кальмодулин /20/.
Факторы патогенности основных
возбудителей гнойных хирургических
инфекций подробно рассмотрены в обзорах /32,
35, 37, 39, 57/.
Наряду с факторами патогенности
бактерии вырабатывают факторы, оказывающие
благоприятное влияние на течение гнойного
процесса. Они продуцируют гидролитические
ферменты, разрушающие некротические ткани,
а также антибиотики, подавляющие рост
других патогенных микроорганизмов.
Например, синегнойная палочка выделяет протеазы
и антибиотик пиоцианазу,
подавляющую рост стафилококков /11/.
Бактерии продуцируют и стимуляторы
иммунитета, скажем, формилпептиды,
стимулирующие фагоцитоз у нейтрофилов/33/. В
качестве примеров можно привести также
бактерийные полисахариды,
повышающие микробоцидность
макрофагов /17/ и N-ацетилглюкозаминил-N-ацетилмурамил-L-аланил-D-изоглутамин,
представляющий собой общий повторяющийся
фрагмент пептидогликана
клеточной стенки всех известных бактерий и
активизирующий практически все
звенья иммунной системы и лейкопоэз,
а также являющийся противовоспалительным
агентом /8/.
Интересным является вопрос об
экологической сукцессии в ране, т.е. о
закономерной смене в ней одной микрофлоры
другой. Поскольку для лечения больных с
гнойными ранами применяют антибиотики,
следует рассматривать только материалы по
смене микрофлоры в экспериментальных
гнойных ранах у животных, у которых
первичное инфицирование происходило
спонтанно и вызывалось дикими штаммами
микроорганизмов, а раны не подвергались
никакому лечебному воздействию. Данилина Е.М.
и соавторы /4/ сообщили, что преобладающей
микрофлорой гнойных ран крыс,
индуцированной введением 8% CaCl2,
до 12-14 дня после операции была
грамположительная кокковая микрофлора,
которая в дальнейшем закономерно
замещалась грамотрицательной микрофлорой.Авторы
предположили, что смена микрофлоры связана
с глубиной разложения некротических тканей.
4. Антибактериальная защита
организма.
4.1.Системы, осуществляющие
антибактериальную защиту организма.
Антибактериальная защита
организма осуществляется системами
неспецифического и специфического
иммунитета. Вспомогательные функции
выполняют система белков острой фазы и
система микроциркуляции раны /5, 9, 22, 33/.
4.2. Система неспецифического
иммунитета.
К системе неспецифического
иммунитета относятся система комплемента (при
ее активации по альтернативному пути),
система пропердина и фагоциты (неиммунный
фагоцитоз и секреция антимикробных
факторов) /26, 33/.
4.3. Система специфического
иммунитета.
К системе специфического
иммунитета относятся система комплемента (при
его активации по классическому пути),
фагоциты (иммунный фагоцитоз), а также В-лимфоциты,
секретируемые ими антитела и Т-лимфоциты /9,
33/.
4.4. Антимикробные факторы
фагоцитов.
Ниже перечисляются
антимикробные факторы фагоцитов (нейтрофилов
и макрофагов) /33/.
1.Кислородзависимые:
1.1. Взаимодействующие с миелопероксидазой
(3. 11. 1. 7) (МПО);
МПО-независимые:
Перекись водорода.
Cупероксид-анион
1.2.3. Радикал гидроксила;
1.2.4. Синглетный
кислород;
1.2.5. Пероксинитрит
анион.
2. Азот-зависимые :
2.1. Оксид азота.
2.2. Диоксид азота.
2.3. Нитрит.
2.4. Нитрат.
3. Кислород- и азот- независимые:
3.1. Щелочной и кислый рН
в фаголизосоме.
3.2. Антибактериальные
белки гранул.
3.2.1. Дефенсины.
3.2.2. Белок, усиливающий
проницаемость бактерий.
3.2.3. Нейтральные
протеиназы.
3.2.4. Лизоцим (3. 2. 1. 17).
3.2.5. Лактоферрин.
3.2.6. Кислые
гидролазы лизосом.
3. 3. Фосфолипаза А2
(3.1.1.4).
3.4. Гистоны.
Далее...
Написать комментарий
| 
