Другой, ставший знаменитым, эксперимент был проведен спустя год [Rose T.S., Rosker M.J., Zewail A.H. // J. Chem. Phys. 1988]. В нем изучалась динамика разрыва связи в молекуле иодистого натрия NaI:
NaI  [Na???I]* [Na???I]*  Na + I
Импульс накачки, действуя на молекулу, находящуюся в основном, ионном, состоянии Na+I-, переводит ее в возбужденное ковалентное состояние NaI. Na + I
Импульс накачки, действуя на молекулу, находящуюся в основном, ионном, состоянии Na+I-, переводит ее в возбужденное ковалентное состояние NaI.
В возбужденной молекуле ядра Na и I начинают двигаться относительно друг друга и, когда расстояние становится равным примерно 6.9 Е, потенциальные энергии ионного и ковалентного состояний выравниваются. После этого молекула имеет две возможности: остаться в неустойчивом ковалентном состоянии и вскоре распасться на нейтральные атомы Na и I или перейти обратно в устойчивое ионное состояние, в котором будут продолжаться колебания ядер. При каждом сближении атомов на критическое расстояние часть молекул распадается на атомы, а часть остается в связанном виде.
Если второй, зондирующий, импульс возбуждает продукт реакции - свободные атомы натрия, - последующий затем сигнал флуоресценции имеет ступенчатую форму: при каждом критическом сближении фрагментов он возрастает за счет распада молекул и появления новых атомов натрия. Если же зондирующий импульс возбуждает переходный комплекс, т.е. колеблющуюся молекулу, сигнал флуоресценции приобретает вид затухающей последовательности всплесков, каждый из которых соответствует критическому сближению ядер при колебаниях. Уменьшение высоты всплесков при каждой последующей бифуркации позволяет определить вероятность распада активированного комплекса. Она составляет около 20%. Кроме того, расстояние между пиками-всплесками показывает период (он составляет около 1.25 пc) колебаний и распадов этого комплекса. Наконец, можно рассчитать и время жизни колеблющейся молекулы: она существует примерно в течение 10 колебаний. Таким образом, меняя время задержки между импульсами и длину волны зондирующего импульса, удается в реальном времени наблюдать переходы между ионным и ковалентным состояниями молекулы NaI и образование атомов натрия при ее диссоциации.
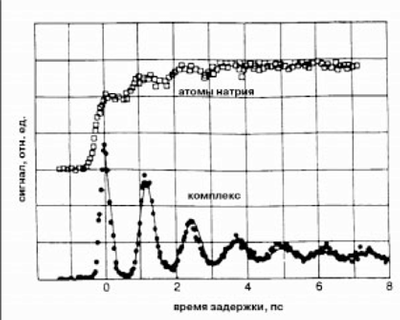 | | Рис.5. Динамика распада активированного комплекса [Na???I]*. Ступенчатое увеличение интенсивности флуоресценции Na*, наблюдаемое при возбуждении продукта реакции - свободного атома натрия, отражает накопление этих атомов при периодической диссоциации переходных комплексов. Последовательное уменьшение амплитуд всплесков при возбуждении активированного комплекса свидетельствует о понижении концентрации возбужденных молекул NaI за счет их периодического распада. (Rose T.S., Rosker M.J., Zewail A.H., 1988.) |
Главный результат работ Зевейла - возможность следить за протеканием элементарных химических реакций в реальном масштабе времени. По сути, им создан новый раздел химии - фемтохимия, которая изучает химические процессы в фемтосекундном временном диапазоне.
Работы Зевейла привели к настоящему взрыву исследований динамики химических реакций. Вот перечень некоторых основных типов реакций, иллюстрирующий возможности фемтосекундной импульсной спектроскопии в исследовании химической динамики:
реакции фотодиссоциации (HgI2, CH3I, NaI);
бимолекулярные реакции
(Br + I2  BrI + I); BrI + I);
реакции изомеризации (цисC6H5CH=CHC6H5  трансC6H5CH= = CHC6H5); трансC6H5CH= = CHC6H5);
реакции элиминирования (CF2ICF2I  C2F4 + I2); C2F4 + I2);
реакции Дильса-Альдера;
реакции с переносом заряда;
реакции внутримолекулярного и межмолекулярного переноса протона (кислотно-основные реакции);
реакции таутомеризации
.
Во всех этих случаях удалось полностью описать динамику образования и распада переходного комплекса в реальном масштабе времени.
Современные достижения фемтохимии уже подробно изложены в обзорных монографиях [Ed. J.Manz and L.Woste, 1995; Ed. M.Chergui, 1996; Ed. V.Sundstrom, 1997].
Cжатие лазерных импульсов до 4 фс означает, что в исследовании химических процессов достигнут нижний временной предел. Дальше укорачивать импульсы бессмысленно, так как даже самые быстрые элементарные реакции длятся не меньше 10 фс. Поэтому развитие метода фемтосекундной спектроскопии будет происходить не вглубь, а путем расширения круга изучаемых объектов.
Созданный Зевейлом метод исследования сверхбыстрых процессов может быть использован не только для анализа реакций в газовой фазе и в молекулярных пучках, но и для изучения процессов в растворах и на межфазных границах. Выяснение механизмов перераспределения энергии в сложных молекулах позволит предсказывать их реакционную способность и создавать новые синтетические методы. Анализ динамики реакций на поверхности может прояснить многое в механизмах действия гетерогенных катализаторов, а применение фемтосекундных импульсов в биохимии - выявить тонкие детали механизмов действия биологически активных молекул.
Другой важный аспект изучения сверхбыстрых процессов связан с возможностью управления ими. Уже первые успехи в изучении динамики реакций в реальном времени навели на мысль, что можно пускать химическую реакцию по заранее запланированному пути и с заданной скоростью. Расчеты дали обнадеживающие результаты: подбирая в сложных последовательностях лазерных импульсов длины их волн и времена задержек, можно концентрировать элементарное возбуждение в любой части молекулы. В некоторых простых случаях удалось экспериментально осуществить селективный разрыв химической связи. Это означает, что в химической динамике появилось новое направление - химия отдельных связей.
Прежде чем техника селективного разрыва или образования отдельных связей найдет применение в практическом химическом синтезе, пройдет еще много времени. Но есть надежда, что лазерное управление химической динамикой когда-нибудь станет общедоступной техникой синтеза, с помощью которой можно будет "вытворять химические чудеса", недоступные обычным препаративным методам. И химики, пользуясь своей самой быстрой в мире фемтосекундной "камерой", смогут снимать неординарные "химические фильмы".
Dantus M., Rosker M.J., Zewail A.H. // J. Chem. Phys. 1987. V.87. P.2395-2397.
Цитируется по: Zewail A.H. // J. Phys. Chem. 1993. V.97. P.12427-12446.
Rose T.S., Rosker M.J., Zewail A.H. // J. Chem. Phys. 1988. V.88. P.6672-6681.
Femtosecond Chemistry / Ed. J.Manz and L.Woste. Weinheim, 1995; Femtochemistry: Ultrafast Chemical and Physical Processes in Molecular Systems / Ed. M.Chergui. Singapore, 1996; Femtochemistry and Femtobiology / Ed. V.Sundstrom. Singapore, 1997
Назад
Написать комментарий
|

