Адсорбция (от лат. ad - на, при и sorbeo - поглощаю) - преимущественное концентрирование молекул газа
или растворенного в жидкости вещества (адсорбата) на поверхности жидкости или твердого тела (адсорбента), а также растворенного
в жидкости вещества на границе ее раздела с газовой фазой. Частный случай сорбции. Один из важнейших типов поверхностных
явлений.
Явление адсорбции связано с тем, что силы межкмолекулярного взаимодействия на границе раздела фаз не скомпенсированы, и, следовательно,
пограничный слой обладает избытком энергии - свободной поверхностной энергией. В результате притяжения поверхностью раздела фаз
находящихся вблизи нее молекул адсорбата свободная поверхностная энергия уменьшается, т. е. процессы адсорбции энергетически выгодны.
В зависимости от характера взаимодействия молекул адсорбата и адсорбента различают физическую адсорбцию и хемосорбцию. Физическая адсорбция
обусловлена силами межмолекулярного взаимодействия и не сопровождается существенным изменением электронной структуры молекул адсорбата. Физическая адсорбция
может быть как монослойной (с образованием мономолекулярного слоя), так и полимолекулярной (многослойной). При адсорбции электролитов из их растворов
обычно возникает двойной электрический слой. Если жидкий адсорбат смачивает пористый адсорбент, то в порах последнего может происходить капиллярная
конденсация. При физической адсорбции адсорбируемые молекулы обычно обладают поверхностной подвижностью.
При хемосорбции между атомами (молекулами) адсорбента и адсорбата образуется химическая связь, т. о. хемосорбцию можно рассматривать
как химическую реакцию, область протекания которой ограничена поверхностным слоем. В некоторых случаях на одной поверхности могут протекать оба типа адсорбции одновременно.
В случае не слишком пористых адсорбентов физическая адсорбция имеет место, как правило, при температуpax ниже критической температуры конденсации адсорбата, хемосорбция же
чаще всего протекает при гораздо более высоких температурах. Однако в некоторых системах физическая адсорбция может протекать при температуpax, значительно превышающих критическую
температуру
конденсации адсорбата. Как и любые химические реакции, процессы хемосорбции носят специфичный характер (т.е. адсорбент хемосорбирует не любые молекулы, а лишь те, которые
вступают в реакцию с атомами поверхности); в некоторых случаях специфичность может проявляться и при физической адсорбции.
Физические характеристики адсорбции. Количественной характеристикой адсорбции является величина Г, представляющая собой избыток адсорбата, приходящийся на
единицу площади поверхностного слоя, по сравнению с количеством адсорбата в единицу объема фазы адсорбента. Отношение 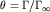 , называется
степенью (или долей) покрытия поверхности (
, называется
степенью (или долей) покрытия поверхности (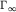 - предельно возможная
величина монослойной адсорбции для данной
системы).
- предельно возможная
величина монослойной адсорбции для данной
системы).
Процессы адсорбции почти всегда сопровождаются выделением теплоты, называемой теплотой адсорбции, которая возрастает с увеличением прочности
связи адсорбат-адсорбент и составляет обычно 8-25 кДж/моль (иногда до 80 кДж/моль) для физической адсорбции и, как правило, превышает 80 кДж/моль при хемосорбции. Если
хемосорбция сопровождается диссоциацией адсорбируемых молекул, может наблюдаться поглощение тепла. По мере заполнения поверхности теплота адсорбции обычно уменьшается в результате
неоднородного распределения свободной энергии на поверхности или латерального взаимодействия молекул в адсорбирующем слое. Для
адсорбентов, обладающих несколькими типами адсорбирующих центров (см. ниже), теплота адсорбции может быть различной для разных типов центров, и распределение
свободной энергии на поверхности является дискретно-неоднородным. При переходе к полимолекулярной адсорбции теплота адсорбции понижается до величины, близкой к теплоте конденсации
адсорбата. Если теплота адсорбции сравнима с поверхностной энергией адсорбента, то в процессе аддсорбции может существенно меняться кристаллическая
структура поверхности твердого тела, причем при физической адсорбции перестройке подвергаются в основном поверхности молекулярных
кристаллов, а в случае хемосорбции изменение поверхностной структуры наблюдается даже для металлов и ионных кристаллов.
Обратный адсорбции процесс, при котором адсорбируемые частицы покидают поверхность адсорбента, называется десорбцией. Десорбция происходит в результате
колебательных
движений адсорбированных молекул вдоль направления действия силы притяжения между адсорбатом и адсорбентом. Период таких колебаний  обычно составляет
обычно составляет 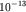 с. Скорость адсорбции и скорость десорбции могут быть рассчитаны методами статистической термодинамики. Скорость
медленных процессов хемосорбции в большинстве случаев описывается уравнением
с. Скорость адсорбции и скорость десорбции могут быть рассчитаны методами статистической термодинамики. Скорость
медленных процессов хемосорбции в большинстве случаев описывается уравнением
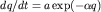
где q - количество адсорбируемого вещества, a - константы, зависящие от температуры. При равенстве скоростей адсорбции и десорбции устанавливается
адсорбционное равновесие. Средняя продолжительность времени, которое частица находится в адсорбированном состоянии в равновесных условиях (время адсорбции), 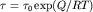 , где Q - теплота адсорбции, R - универсальная газовая постоянная, Т - абсолютная температура.
Принято считать, что адсорбция имеет место в том случае, когда
, где Q - теплота адсорбции, R - универсальная газовая постоянная, Т - абсолютная температура.
Принято считать, что адсорбция имеет место в том случае, когда  достигает величины нескольких периодов колебаний адсорбированной молекулы
- время, за которое между ней и поверхностью успевает установиться энергетическое равновесие. Обычно время физической адсорбции составляет
достигает величины нескольких периодов колебаний адсорбированной молекулы
- время, за которое между ней и поверхностью успевает установиться энергетическое равновесие. Обычно время физической адсорбции составляет  с,
а время хемосорбции - свыше
с,
а время хемосорбции - свыше 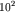 с. Время адсорбции служит критерием обратимости процесса адсорбции.
с. Время адсорбции служит критерием обратимости процесса адсорбции.

