|
Измайлов С.Г., Горбунов С.М., Измайлов Г.А., Заиконникова И.В. , Резник В.С., Абдрахманова Н.Г., Пашкуров Н.Г., Кедрин М.Ю., Герасимова М.Х., Гараев В.Н., Измайлов А.Г., Подушкина И.В., Эвранова Г.Б., Муслинкин А.А. Военно-медицинский институт Нижегородской медицинской академии, Казанский государственный медицинский университет, Институт органической и физической химии Казанского научного центра РАН, Казанская медицинская академия
АНТИБИОТИКИ И ХИМИОТЕРАПИЯ, 1999-N8, стр. 12-17. В начало...
В эксперименте на разных видах животных изучены фармако-токсикологические свойства нового пиримидинового производного - ксимедона. Энтеральное введение препарата, благоприятно действовало при лечении термических ожогов, кожных и желудочных послеоперационных ран. Полученные результаты позволяют рекомендовать ксимедон для использования в клинической практике.Ключевые слова:
Ксимедон является оригинальным пиримидиновым производным, синтезированным в ИОФХ им. А.Е. Арбузова. Проведенное нами ранее экспериментальное изучение показало, что ксимедон является эффективным стимулятором процессов репаративной регенерации тканей [1-3].
Задачами настоящего доклинического исследования ксимедона явились изучение его фармако-токсикологических свойств, экспериментальное обоснование использования препарата для лечения термических ожогов кожи, в том числе оценка эффективности энтерального применения ксимедона по влиянию на процесс заживления кожных послеоперационных ран и ран пищеварительного тракта.
Работа выполнена на 6 беспородных взрослых собаках, 120 кроликах породы шиншилла, 364 мышах, 362 беспородных крысах, 194 крысах линии Вистар и 372 морских свинках. При изучении острой токсичности определяли LD50 ксимедона для морских свинок, мышей и крыс. При изучении безвредности препарат вводили крысам перорально в терапевтической дозе в течение 6 месяцев. Термические ожоги III степени вызывали у морских свинок контактным способом, с поражением 4-5% поверхности тела. Изучение влияния ксимедона на заживление ран пищеварительного тракта проводили на кроликах.
Данные проведенных фармако-токсикологических исследований ксимедона свидетельствуют о его низкой токсичности: так, LD50 для морских свинок составила 14,3, для мышей - 4,2 и для крыс - 3,8 мг/кг. Введение ксимедона в летальных дозах вызывало угнетение двигательной активности с последующим развитием клонико-тонических судорог и кратковременного опистотонуса. Смерть животных наступала от остановки дыхания. У морских свинок при введении летальных доз препарата внутрь наблюдалась диарея. Патологоанатомическое исследование погибших животных выявило полнокровие органов, а у морских свинок, кроме того, выявлено расширение желудка и кишечника, особенно слепой кишки.
При введении животным токсических доз признаки отравления были более продолжительными, судорожное состояние менее выражено. Выжившие животные практически не отличались от интактных уже на следующий день.
Однократное введение внутрь ксимедона 3 половозрелым беспородным собакам в дозе 12,5 г/кг (500-кратная суточная доза для человека) не выявило каких-либо изменений их состояния по сравнению с 3 контрольными животными. Последующее (через сутки) патологоанатомическое вскрытие не обнаружило макроскопических изменений в органах и тканях подопытных собак.
Данные опытов по изучению безвредности препарата свидетельствуют о том, что ксимедон, вводимый перорально в терапевтической дозе в течение 6 месяцев, не вызывал заметного токсического влияния на организм подопытных крыс, а именно: не вызывал падения веса на всем протяжении опыта, не влиял на диурез, не изменял функциональной активности печени, не вызывал достоверных сдвигов в биохимических параметрах крови опытных крыс по сравнению с контрольными и не вызывал макро- и микроскопических изменений во внутренних органах.
Введение ксимедона белым мышам способствовало ускорению заживления обширных ран на 18,3-44,5% по сравнению с контрольными, в зависимости от дозы, пути введения и схемы лечения. Наилучшие результаты получены при применении ксимедона в форме присыпки на рану однократно: ускорение заживления достигало 44,5%.
Сравнение сроков заживления ран при введении ксимедона перорально, внутрибрюшинно и внутримышечно показывает преимущества перорального введения, причем сроки заживления при этом пути введения достоверно меньше, чем при двух других путях введения.
У морских свинок с ожогами III степени и площадью ожога 4-5% поверхности тела на 2-й день после нанесения ожога формировался толстый плотный первичный ожоговый струп серовато-коричневого цвета. Начиная с 7-9 дня струп отторгался по краям раневой поверхности. При применении ксимедона струп отпадал на 1,5 дня раньше, чем у контрольных животных. Форма ожоговой раны после отпадения струпа претерпевала существенные изменения, однако во всех сериях опытов эти изменения были стереотипны, разница выражалась лишь в темпах контракции ран [2]. Полная эпителизация ожоговой раны наблюдалась у свинок, получавших ксимедон - на 24-е сутки, при лечении метилурацилом - на 27-е, в то время как в контроле - на 29-е сутки, т.е. введение ксимедона ускоряло заживление ожоговых ран на 19,7% по сравнению с контролем и на 12,4% - по сравнению с метилурацилом.
Гистохимические исследования показали, что на 3-й день после нанесения ожога у животных, получавших ксимедон и метилурацил, наблюдаются, в отличие от контроля, повышение активности ферментов, в том числе гидролитических (кислой фосфатазы), в клеточных элементах раневого дефекта и окружающих его тканей. Ксимедон оказывал благоприятное влияние на течение раневого процесса в более ранние сроки (на 3-7-й день) по сравнению с морскими свинками, получавшими метилурацил, или контрольной группы. Это проявлялось в ускоренном формировании грануляционной ткани, более выраженной активности ферментов в краевых участках ран, что свидетельствует о более выраженной потенциальной способности к регенерации.
Изучение динамики биохимических показателей белкового обмена под влиянием ксимедона показало следующее: ксимедон способствует сохранению количества общего белка в сыворотке крови; вызывает быструю нормализацию относительного количества альбумина, а также 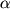 1- и 1- и 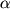 2-глобулинов по сравнению с контролем; гипо- и диспротеинемия ликвидируются раньше, чем у животных, получавших метилурацил; содержание мочевины в сыворотке крови не изменяется, что может свидетельствовать о сохранении белка в тканях. 2-глобулинов по сравнению с контролем; гипо- и диспротеинемия ликвидируются раньше, чем у животных, получавших метилурацил; содержание мочевины в сыворотке крови не изменяется, что может свидетельствовать о сохранении белка в тканях.
Исследования показали, что при нанесении ожога изменяется фагоцитарная функция, причем в наибольшей степени снижается показатель завершенности фагоцитоза (ПЗФ) - до 44,9% от нормы. У животных, получавших ксимедон, повышались все изученные показатели фагоцитарной реакции, причем в наибольшей степени повышался ПЗФ (до 86,3 5,9%). Метилурацил также стимулировал фагоцитоз, однако достоверно в меньшей мере, чем ксимедон. Под влиянием ксимедона максимальный лейкоцитоз к 3 дню эксперимента составлял 11000 в 1 мм3 крови. У животных, получавших метилурацил, на всех сроках наблюдения лейкоцитоз был выражен в меньшей степени по сравнению с животными, получавшими ксимедон. Таким образом, введение животным ксимедона способствует развитию умеренного лейкоцитоза и значительному усилению фагоцитарной активности лейкоцитов, особенно в завершающей стадии фагоцитоза, что играет важную роль в лизисе микроорганизмов.
Исследование ряда показателей белкового обмена у свинок с ожогом III-Б степени и площадью поражения 4-5% показало, что данная экспериментальная модель термического ожога создает необходимый фон для изучения влияния на организм ксимедона. Об этом свидетельствует достоверное снижение содержания общего белка в сыворотке крови, происходящее в основном за счет снижения количества альбумина: кривые абсолютного количества альбуминов и общего белка сыворотки обожженных животных располагаются практически параллельно друг другу.
Влияние ксимедона на упруго-прочностные характеристики послеоперационного рубца изучались на крысах также в сравнении с метилурацилом. С первого дня после операции животные обеих опытных групп получали соответственно 10% раствор ксимедона (500 мг/кг массы тела) и 100 мг/кг метилурацила, которые растворяли в изотоническом растворе хлорида натрия и вводили тонким зондом через рот в желудок один раз в сутки. Животным контрольной группы вводили только физиологический раствор (5 мл/кг). На 5, 7, 9, 14 и 21-й дни забирался материал для тензиометрического и гистологического исследований. Изучение антимикробного действия ксимедона с целью возможности включения его в состав разработанного нами протектора ран проводилось методом серийных разведений на жидкой питательной среде (данные не приводятся).
Опыты по изучению влияния различных доз ксимедона (при его энтеральном введении) на скорость заживления послеоперационных кожных ран дали следующие результаты. Напряжение разрыва при дозах препарата от 50 до 250 мг было практически одинаковым (р<0,05), при дозе 500 мг происходило статистически достоверное увеличение напряжения разрыва рубца по сравнению с предыдущими дозами ксимедона (табл. 1).
| Таблица 1. Прочность послеоперационного рубца, в зависимости от дозы ксимедона, на 5-й день после операции (М m) |
| Показатель тензиометрии |
Доза, мг/кг |
| 50 |
100 |
250 |
500 |
750 |
Напряжение разрыва, 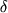 В*104 Па В*104 Па |
33,0 2,8 |
31,3 3,1 |
31,8 3,2 |
44,0 3,2
р<0,05
р1<0,05
р2<0,05 |
39,8 8,5
р3>0,05 |
Примечание: р - достоверность разности средних по сравнению с 50 мг; р1 - по сравнению с 100 мг; р2 - по сравнению с 250 мг; р3 - по сравнению с 500 мг.
Прочность послеоперационного рубца при дозах 500 и 750 мг была почти идентична (р<0,05), из этих доз была выбрана первая, так как при ней достигалась наибольшая прочность послеоперационного рубца.
При анализе диаграмм растяжения лоскутов кожи констатировано, что ксимедон оказывает заметное положительное влияние на ускорение заживления кожных ран, выражающееся в повышении прочности и упругости послеоперационных рубцов (табл. 2).
Таблица 2. Сравнительные показатели напряжений разрыва (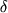 В*104 Па) послеоперационных рубцов (М m) В*104 Па) послеоперационных рубцов (М m) |
| Группа животных |
Дни после операции |
| 5-й |
7-й |
9-й |
14-й |
21-й |
| Kонтрольная |
21,6 1,6 |
34,7 2,2 |
75,7 3,0 |
114,9 11,5 |
228,0 84,9 |
| Опытная |
33,9 1,9 |
50,7 1,7 |
94,3 2,1 |
142,2 11,2 |
379,5 40,5 |
| p |
<0,001 |
<0,001 |
<0,001 |
>0,05 |
>0,05 |
Из табл. 2 видно, что напряжение разрыва в опытной группе (с применением ксимедона) на 5, 7 и 9-й дни после операции по сравнению с контрольной группой больше соответственно на 57,0, 31,6 и 19,7% (р<0,001). Однако, начиная с 7-го дня, происходило постепенное выравнивание показателя прочности сращения краев раны между исследуемыми группами животных и на 14 и 21-й дни различие в напряжении разрыва рубца становилось статистически недостоверным (р>0,05). Мы объясняем это тем, что ксимедон не нарушает естественный ход течения раневого процесса и в основном проявляет действие на ранних сроках заживления раны, поскольку он способен усиливать фагоцитарную активность лейкоцитов, уменьшать воспаление, повышать функциональную активность клеток соединительной ткани и усиливать синтез коллагена и нуклеиновых кислот.
Далее...
Написать комментарий
|

